세포는 영양이 부족해지면 분해효소를 지닌 세포 소기관이 불필요한 세포 소기관을 분해 및 재활용하는데, 이를 자가포식이라 한다. 자가포식이 제대로 일어나지 않으면, 세포는 충분한 에너지를 확보할 수 없어 죽게 된다. 일본의 오스미 요시노리(Yoshinori Ohsum)가 세포 자가포식의 메커니즘을 규명한 공로로 2016년 노벨생리의학상을 받았을 만큼 생명과학의 매우 중요한 연구분야로 생명현상을 지속하기에 적합한 환경을 유지하는데 핵심적인 역할을 한다.
기존 연구에서는 자가포식에 관여하는 두 세포 소기관을 관찰하기 위해 형광 단백질을 주로 이용해왔다. 그러나 자가포식 과정 중 분해 효소로 인해 형광 단백질이 함께 분해되는 탓에 자가포식 현상을 안정적으로 관찰하는 데 어려움이 있었다.
세포 자가포식은 리소좀과 같이 분해 효소를 지닌 소기관과 분해될 다른 소기관이 만나 이루어진다. 연구진은 분해 대상인 여러 소기관 중, 미토콘드리아를 주목했다. 미토콘드리아는 퇴행성 뇌질환과 연관이 깊은데, 많은 에너지를 사용하는 뇌세포에서 미토콘드리아가 고장 난 채 적절하게 분해되지 않으면 퇴행성 뇌질환으로 이어질 수 있기 때문이다.
IBS 복잡계 자기조립 연구단 연구진(김기문 단장·박경민 연구위원)은 강력한 형광 분자 결합쌍인 쿠커비투릴 분자와 아다만탄아민 분자의 특이적 결합 원리를 이용했다. 자가포식 과정에서 함께 사라지는 형광 단백질과 달리, 연구진이 개발한 형광 분자 결합쌍으로는 세포 소기관 각각의 움직임 뿐 아니라 두 소기관의 융합 과정도 확인할 수 있다. 세포 자가포식의 전 과정을 실시간으로 살펴보는 것이 가능해진 셈이다.
김기문 IBS 복잡계 자기조립 연구단장은 "형광 분자 결합쌍을 이용한 바이오 이미징 기술은 복잡한 세포 기작을 보다 세심히 연구할 수 있는 길을 열 것"이라 말했다. 이번 연구에서 개발한 이미징 기술은 향후 암, 감염병, 노화 등의 치료와 신약 개발 연구 분야 발전에 기여할 것으로 기대된다.
이번 연구결과는 독일 응용화학회지(Angewandte Chemie International Edition, IF 11.994) 온라인판에 지난달 25일에 게재됐다.이용민 기자
<저작권자ⓒ대전일보사. 무단전재-재배포 금지>


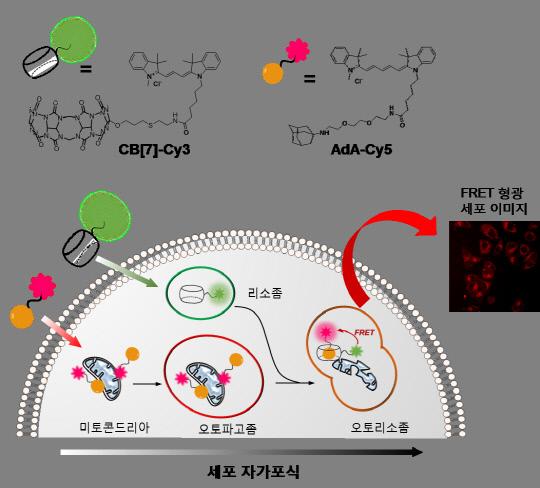
![위의 그래프에서 쿠커비투릴(CB[7]-cy3)은 500nm 중반대에서, 아다만탄아민(AdA-cy5)은 약 660nm 정도의 파장에서 뚜렷이 감지될 만한 형광을 나타냄을 확인할 수 있다. 세포 자가포식이 일어남에 따라 리소좀과 미토콘드리아가 융합(Mix)하면 이 둘에 붙어있던 두 형광분자가 가까워진다. 이때 에너지 전이(FRET)가 일어나 아다만탄아민을 볼 수 있는 비슷한 파장의 영역에서 새로운 강도의 형광이 나타난다. 에너지 전이로 인한 새로운 형광 덕분에 미토콘드리아와 리소좀이 융합한 과정을 관찰할 수 있는 것이다. 자료=IBS 제공](https://cdn.daejonilbo.com/news/photo/201802/1300828_234620_1816.jpg)